
البنزين العطري


البنزين هو عباره عن مادة سائلة متطايرة , عديمة اللون لها رائحه عطرية .
تركيب البنزين افترض العالم الالماني كيكيولي عام 1865م ان ذرات الكربون الست في جزيء
البنزين مرتية على شكل حلقة سداسية, وكل ذرة ترتبط برابطة احادية مع ذرة
هيدروجين , كما هو موضح في الاشكال التالية :

 الرنين في البنزين
الرنين في البنزين 
لو رجعنا لصيغة كيكيولي سيتضح لنا بان تفاعلات البنزين تكون من نوع تفاعلات
الاضافة لوجود الروابط الثنائية , ولكن اتضح بعد ذلك بان البنزين يختلف
كليا في خواصه عن خواص الالكينات , فهو يتفاعل غالبا بالاستبدال. ولذلك عدل
كيكيولي فرضه الاولواعتبر ان للبنزين صيغتين بنائيتين كالتالي :

الصيغة الرنينية في البنزين
نلاحظ ان موقع الرابطة الثنائية بين ذرتي الكربون في الصيغتين تتغير , ولكن
ذرات الكربون تبقى ثابته اي ان الاختلاف ينحصر في موقع الالكترونات بينما
موقع الذرات يبقى ثابت بالنسبة لبعضها .

والسبب في وضع الصيغة الرنينيه , هو طول الرابط في البنزين حيث ان طول
الرابطة في البنزين ( 0.140 نانومتر ) اقصر من الرابطة الاحادية ( 0.154
نانومتر ) واطول من الرابطة الثنائية ( 0.134 نانومتر ) .
اي ان البنزين يحتوي على ست روابط بين ذرات الكربون متماثلة في القوة والمسافة بينهما ثابتة = 0.140 نانومتر .
وان كل ذرة منها تستخدم فلكان من النوع SP2 للترابط مع ذرتي الكربون
المتجاورتين وتستخدم الثالث للترابط مع ذرة الهيدروجين وتبقى لكل ذرة كربون
الكترون واحد في الفلك P النقي غير المهجن والمتعامد على مستوى الحلقة .
كما هو موضح في الشكل التالية :

وبالتالي يكون لكل الكترون تاثير من وعلى الاكترونات التي تكون على جانبية كما هو موضح في الشكل التالي :

ونتيجة لتداخل هذه الافلاك تتكون سحابة الكترونية من النوع باي فوق واسفل الحلقة :
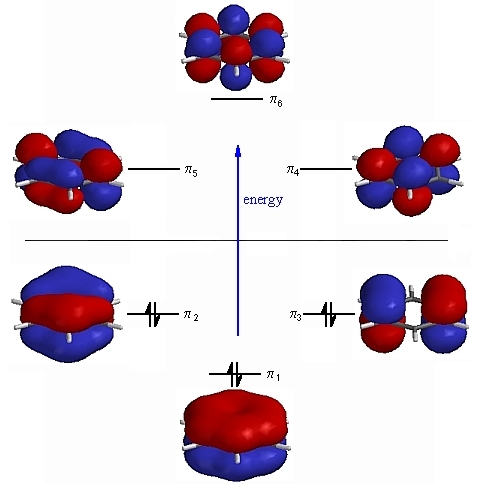
هذه الشحنة الالكترونية منتشره بالتساوي وذلك لعدم تموضعها فهي ملك لجميع ذرات الحلقة في نظام مغلق وليست متمركزة بين ذرات معينة .
لذلك وصف الرنين بانه هو الحالة او الوضع الذي لا نستطيع فيه تفسير كل خواص الجزيء بواسطة صيغة الكترونيه واحده . وقد اصبح مقبولا لدى العاملين في مجال الكيمياء هذه الصيغة :
 طرق تحضير البنزين :
طرق تحضير البنزين : 1. يمكن تحضيرة من التقطير التجزيئي للنفط وقطران الفحم الحجري .
2. من بلمرة الاستيلين مع الية التفاعل:

3- بتقطير الفينول مع مسحوق الخارصين .
 تفاعلات البنزين : · تفاعلات الاستبدال :
تفاعلات البنزين : · تفاعلات الاستبدال : نظرا لثبات البنزين العطري فان معظم تفاعلاته تتم بالاستبدال مع بقاء ترابط ذرات الكربون في حلقة البنزين كما هي وذلك مثل :
1- النترته (Nitration ) : وهي احلال مجموعة نيترو ( -NO2 ) محل ذرة هيدروجين في حلقة البنزين , وذلك
عند تدفئة البنزين مع مخلوط من حمض النيتريك المركز وحمض الكبريتيك المركز
الذي يستخدم كعامل حفاز فينتج نيتروبنزين .
 2- السلفنه (Sulfonation ) :
2- السلفنه (Sulfonation ) : وهي احلال مجموعة السلفونيك ( -SO3H ) محل ذرة هيدروجين في حلقة البنزين .
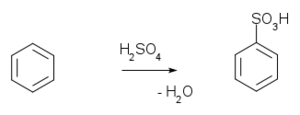 3- الهلجنة (Halogenation ) :
3- الهلجنة (Halogenation ) : وهي احلال ذرة هالوجين او اكثر محل ذرة هيدروجين او اكثر في حلقة البنزين ,
ويتم ذلك بتفاعل الهالوجين مع البنزين في وجود عامل مساعد مثل الحديد او
بروميد الحديد الثلاثي وبعيدا عن ضوء الشمس المباشر .
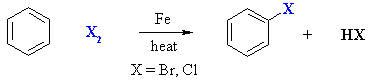 4- الالكلة (alkylation ) :
4- الالكلة (alkylation ) : وهي احلال مجموعة الكيل محل ذرة هيدروجين في البنزين . وذلك بتسخين البنزين
مع هاليد الالكيل ( R-X ) حيث X عبارة عن ذرة هالوجين و R مجموعة الكيل
تختلف باختلاف عدد ذرات الكربون , في وجود عامل مساعد AlCl3 . ويسمى هذا
التفاعل بتفاعل فريدل كرافت (Friedel-Crafts alkylation ) .

وقد تحتوي R على مجموعة كربونيل فتسمى (Friedel-Crafts acylation )
 · تفاعلات الاضافة :
· تفاعلات الاضافة : يتفاعل البنزين بالاضافة في بعض الحالات وذلك في ظروف خاصة حيث تحتاج هذه التفاعلات الى طاقة كبيرة .
1. في ضوء الشمس المباشر يتفاعل البنزين مع الكلور فيتكون سداسي كلورو
الهكسان الحلقي ( الجامكسان ) والذي يستخدم كمبيد حشري , وهذا التفاعل يتم
على خطوات .

2. يتفاعل البنزين مع الهيدروجين بالاضافة تحت ظروف خاصة ( في وجود عامل
مساعد مثل البلاتين المجزأ عند 150° س ) ويتكون الهكسان الحلقي .
 الخواص الفيزيائية للبنزين
الخواص الفيزيائية للبنزين 1. سائل عديم اللون له رائحه مميزة , وبخاره سام .

2. لا يذوب في الماء ولكنه يذوب في المذيبات العضوية مثل الايثر والكحول .
3. عند 20 درجة سيليزية تكون كثافته النسبية 0.88 ودرجة غليانه 80.1 ويتجمد عند 5.5 على شكل بلورات بيضاء .
4. يشتعل بلهب ساطع مدخن .

5. يعتبر من المذيبات الهامة لانه يذيب كثيرا من المواد العضويه وبعض العناصر كاليود والفوسفور .
استخدامات البنزين 1. يستخدم كمذيب في اذابة الدهون والزيوت وغيرها من المواد العضوية التي لا
تذوب في الماء ولهذا يستخدم على نطاق واسع في التنظيف الجاف .
2. يحضر منه النيترو بنزين والطولوين التي تستخدم في تحضير العقاقير الطبية والمفرقعات والاصباغ .



3. يستخدم في تحضير المبيدات الحشرية مثل الجامكسان ومسحوق الـ د. د. ت .
مشتقات البنزينجميع ذرات الهيدروجين في جزيء البنزين متكافئة من جيث الموقع , ولذلك فان
استبدال اي ذرة منها بذرة او مجموعة يؤدي الى تكوين نفس المركب . والصورة
التالية توضح بعض من مشتقات البنزين :

وعند استبدال ذرتين من الهيدروجين في جزيء البنزين بذرتين او مجموعتين فانه
يتكون ثلاث متشابهات مختلفه , اورثو , ميتا وبارا , وسبب هذا الاختلاف
يعود الى مواقعها النسبية كالتالي :

وهناك مشتقات تحتوي على اكثر من تفرعين كالتالي :

المركب ( 1 ) 4,2,1 - ثلاثي كلورو بنزين .
المركب ( 2 ) 6,2 - ثنائي برومو فينول .
المركب ( 3 ) 5,3 - ثنائي برومو فينول .
